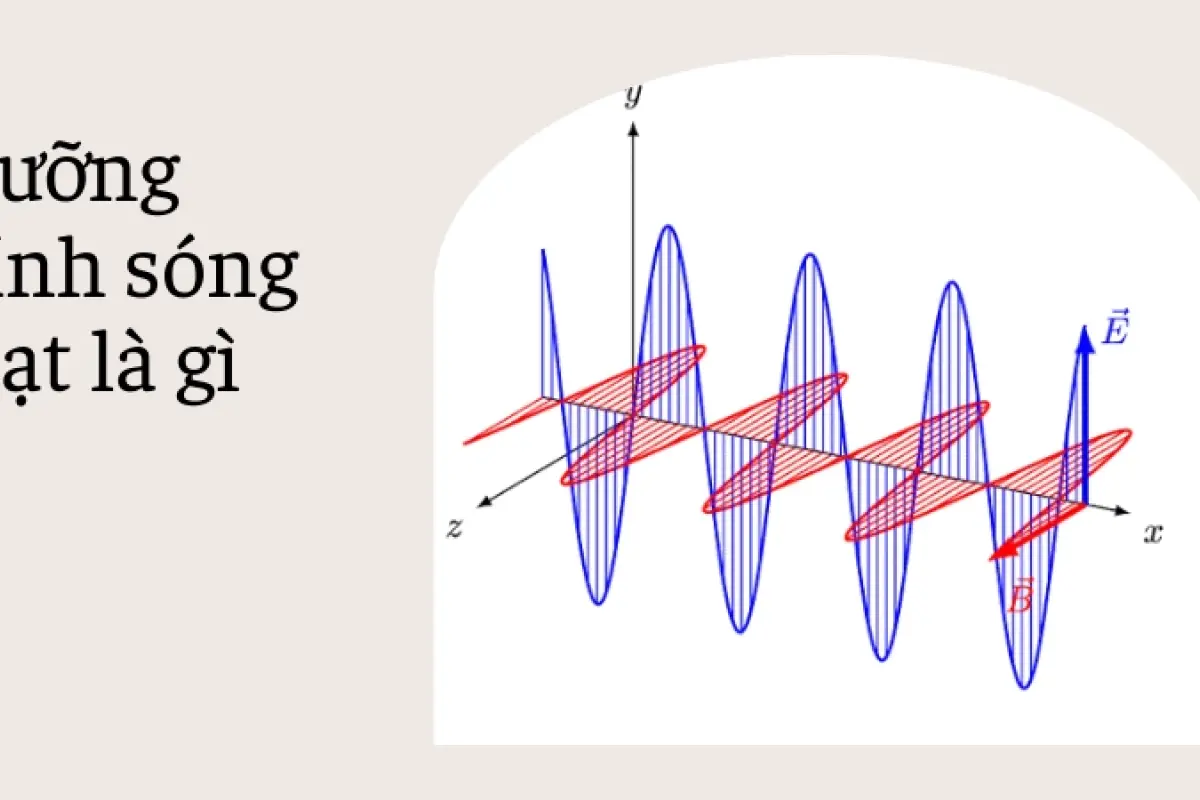

Bản chất lưỡng tính sóng hạt và bí ẩn của vật lý hiện đại
Bản chất lưỡng tính sóng hạt là chìa khóa mở ra cánh cửa vật lý hiện đại. Khám phá sự kết hợp kỳ lạ giữa sóng và hạt giúp bạn làm chủ kiến thức vũ trụ.

Thuyết vướng mắc lượng tử khiến khoa học tranh cãi
Khám phá thuyết vướng mắc lượng tử và những tranh cãi nảy lửa trong giới khoa học. Tìm hiểu sự kỳ quái của vật lý hiện đại vượt xa mọi giới hạn tư duy.
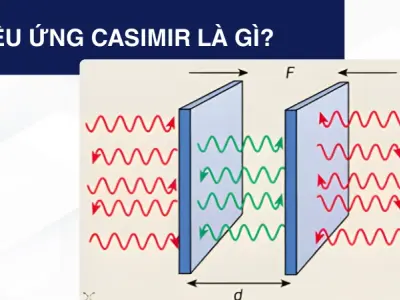
Hiệu ứng Casimir và bí ẩn năng lượng từ chân không lượng tử
Hiệu ứng Casimir chứng minh chân không không hề trống rỗng. Khám phá cơ chế lực hút lượng tử, những tranh cãi khoa học và ứng dụng đột phá trong công nghệ.

Hé lộ về chồng chất lượng tử làm đảo lộn tư duy con người
Khám phá bí ẩn chồng chất lượng tử và cách nó thách thức mọi định luật vật lý truyền thống, mở ra kỷ nguyên mới cho tư duy và công nghệ của nhân loại.
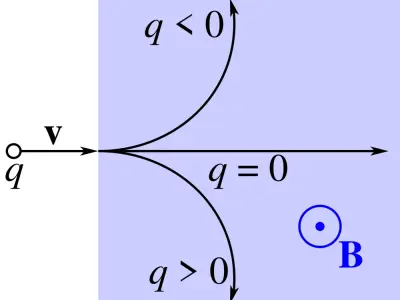
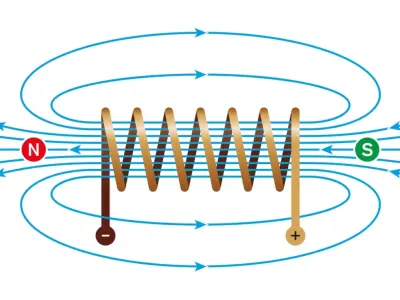
Sơ đồ quy tắc bàn tay trái xác định chiều của lực Lorentz
Khám phá chi tiết về đường sức từ của nam châm để hiểu rõ quy luật vận hành của từ trường. Bài viết cung cấp kiến thức chuẩn xác kèm bộ hình ảnh minh họa sắc nét.

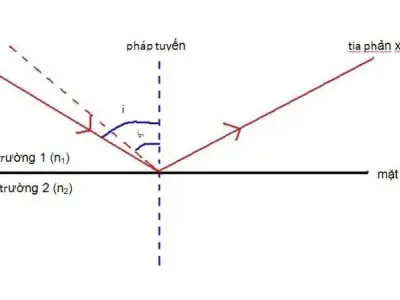
Bộ ảnh tán sắc và khúc xạ ánh sáng qua lăng kính cực nét
Khám phá hiện tượng khúc xạ ánh sáng qua lăng kính và bí ẩn của dải màu cầu vồng. Tìm hiểu lý thuyết, sơ đồ và hình ảnh thực tế sống động ngay tại đây.
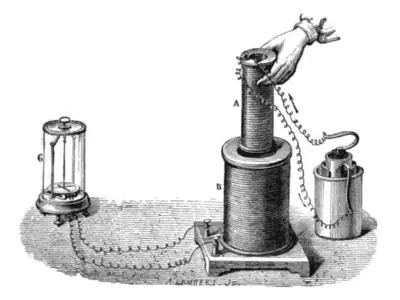
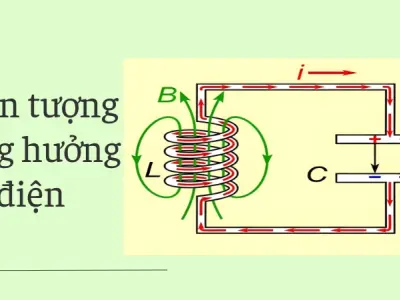
Bộ ảnh minh họa hiện tượng cảm ứng điện từ faraday cực nét
Khám phá nguyên lý cảm ứng điện từ Faraday qua bộ sưu tập hình ảnh trực quan. Tìm hiểu định luật và ứng dụng thực tiễn của hiện tượng vật lý kỳ diệu này ngay.
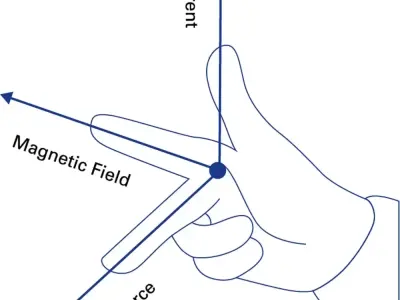
Sơ đồ biểu diễn hình ảnh lực lorentz chi tiết, dễ hiểu
Khám phá định nghĩa lực Lorentz và bộ sưu tập sơ đồ trực quan nhất. Nắm vững công thức, quy tắc bàn tay trái và ứng dụng của lực Lorentz trong vật lý.
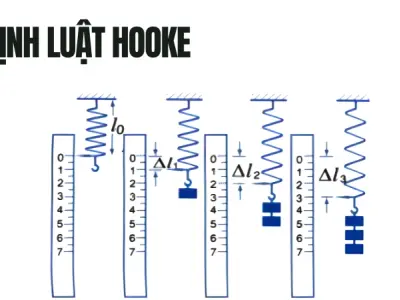
Định luật Hooke và bí mật của lực đàn hồi trong vật lý
Định luật Hooke và những kiến thức vật lý thú vị về lực đàn hồi. Khám phá ngay công thức, ứng dụng thực tế và các lưu ý quan trọng để làm chủ kiến thức này.

Khám phá vẻ đẹp máy gia tốc hạt Large Hadron Collider
Khám phá máy gia tốc hạt Large Hadron Collider của CERN qua bộ sưu tập hình ảnh sắc nét, giúp bạn hiểu rõ cấu tạo và các thí nghiệm tìm kiếm hạt Higgs.

Sơ đồ cấu tạo hình ảnh hạt nhân nguyên tử chi tiết nhất
2026-01-14 21:57:23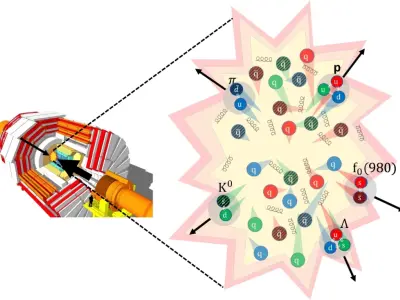
Khám phá cấu trúc hạt quark trong proton qua bộ ảnh chi tiết
2026-01-14 21:56:14
Bí ẩn vật lý về những ứng dụng phi thường của vật lý hạt nhân
2024-03-30 17:35:14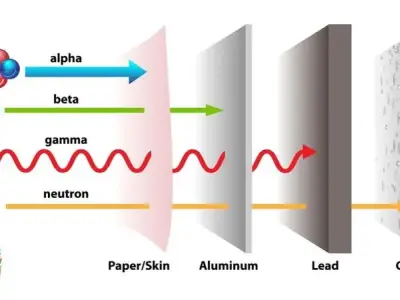
Khám phá bức xạ Alpha, Beta và Gamma
2024-03-28 16:41:03Vật Lý - Nơi hội tụ tri thức, thắp sáng tương lai khoa học
Trong thời đại tri thức bùng nổ, việc tiếp cận nguồn thông tin chính xác và chuyên sâu về khoa học, đặc biệt là vật lý, trở thành nhu cầu thiết yếu. Chúng tôi, tại Vật Lý, tự hào là cổng thông tin hàng đầu, mang đến kho tàng kiến thức đa dạng từ vật lý cổ điển đến những lĩnh vực tiên tiến như cơ học lượng tử hay vật lý hạt nhân. Với sứ mệnh chuẩn hóa nội dung và đồng hành cùng người học, Vật Lý cam kết cung cấp những tài liệu đáng tin cậy, được biên soạn bởi đội ngũ chuyên gia giàu kinh nghiệm.
Là thư viện số uy tín, chúng tôi không chỉ dừng lại ở việc cung cấp thông tin mà còn xây dựng một cộng đồng đam mê khoa học, nơi người dùng có thể học hỏi, trao đổi và khám phá. Dù bạn là học sinh, sinh viên hay nhà nghiên cứu, Vật Lý luôn sẵn sàng trở thành người bạn đồng hành trên hành trình chinh phục tri thức.
Sứ mệnh và Giá trị khác biệt của Vật Lý
Chúng tôi hiểu rằng, trong bối cảnh thông tin tràn lan, việc tiếp cận nguồn tài liệu đáng tin cậy là một thách thức lớn. Vì vậy, Vật Lý đặt sứ mệnh chuẩn hóa kiến thức lên hàng đầu, đảm bảo mọi nội dung đều được kiểm chứng bởi các chuyên gia đầu ngành. Mỗi bài viết, tài liệu hay đề thi trên nền tảng đều được xây dựng với sự tỉ mỉ và chính xác cao nhất, nhằm mang lại giá trị thực tiễn cho người dùng.
Sự khác biệt của chúng tôi nằm ở cam kết bảo vệ quyền lợi người học. Không chỉ cung cấp nội dung miễn phí và dễ tiếp cận, Vật Lý còn xây dựng các công cụ hỗ trợ như hệ thống câu hỏi, bài tập thực hành và phản hồi nhanh chóng từ đội ngũ chuyên gia. Chúng tôi tin rằng tri thức không chỉ là tài sản mà còn là chìa khóa mở ra cánh cửa tương lai.
Kho tàng tri thức đa dạng tại Vật Lý
Hãy cùng khám phá hệ sinh thái nội dung phong phú tại Vật Lý, nơi bạn sẽ tìm thấy mọi khía cạnh của khoa học vật lý được trình bày một cách dễ hiểu và chuyên sâu. Từ những khái niệm cơ bản đến các chủ đề nâng cao, chúng tôi đã xây dựng một thư viện số toàn diện để đáp ứng mọi nhu cầu học tập và nghiên cứu. Dưới đây là những cụm chủ đề nổi bật mà bạn không thể bỏ qua:
- Vật lý cổ điển: Tập trung vào các nguyên lý cơ bản, từ cơ học đến nhiệt học, mang lại nền tảng vững chắc cho người học với những bài giảng chi tiết và dễ áp dụng.
- Cơ học lượng tử: Khám phá thế giới vi mô với các lý thuyết tiên tiến, được giải thích rõ ràng, phù hợp cho cả người mới bắt đầu và nhà nghiên cứu.
- Điện động học và từ học: Cung cấp kiến thức chuyên sâu về điện và từ, với các bài tập thực tiễn giúp người học nắm vững ứng dụng trong công nghệ.
- Vật lý nguyên tử, phân tử và quang học: Phân tích các hiện tượng ánh sáng và cấu trúc vi mô, mở ra góc nhìn mới về thế giới xung quanh.
- Vật lý hạt nhân và hạt cơ bản: Đi sâu vào bản chất của vũ trụ với những nội dung cập nhật từ các nghiên cứu mới nhất, truyền cảm hứng cho những ai đam mê khám phá.
- Đề thi và tài liệu ôn luyện: Bộ sưu tập đề thi phong phú, được biên soạn kỹ lưỡng, hỗ trợ người học đạt kết quả cao trong các kỳ thi quan trọng.
Đội ngũ chuyên gia tận tâm tại Vật Lý
Đứng sau thành công của Vật Lý là đội ngũ biên tập viên và chuyên gia đầy tâm huyết, luôn đặt chất lượng nội dung lên hàng đầu. Dẫn dắt chúng tôi là bà Nguyễn Thị Thanh Tú – Nhà sáng lập kiêm Giám đốc Điều hành – người mang trong mình niềm đam mê mãnh liệt với giáo dục. Với hơn 5 năm kinh nghiệm, bà đã xây dựng Vật Lý trở thành một nền tảng đáng tin cậy, nơi tri thức được lan tỏa một cách ý nghĩa.
Triết lý làm nghề của chúng tôi là sự tận tâm và không ngừng đổi mới. Dưới đây là danh sách những thành viên chủ chốt trong đội ngũ chuyên môn:
- Nguyễn Thị Thanh Tú: Nhà sáng lập, chuyên gia giáo dục với tầm nhìn chiến lược trong việc xây dựng nội dung tri thức.
- Duy Khang: Chuyên gia về các lý thuyết nâng cao, đóng góp lớn trong việc phổ biến kiến thức phức tạp một cách dễ hiểu.
- Hằng Nga: Chuyên gia biên soạn tài liệu ôn luyện, đảm bảo chất lượng các bộ đề thi đạt chuẩn.
- Kiều Anh: Chuyên gia về ứng dụng thực tiễn, mang đến góc nhìn gần gũi trong các chủ đề kỹ thuật.
- Mẫn Nhi: Chuyên gia về nền tảng cơ bản, đồng thời đảm nhiệm sản xuất nội dung hình ảnh sáng tạo.
- Thanh Tùng: Chuyên gia nghiên cứu các lĩnh vực tiên tiến, đóng góp nội dung và hình ảnh chất lượng cao.
- Vũ Hà: Chuyên gia phân tích chuyên sâu, hỗ trợ xây dựng các bài viết mang tính đột phá.
- Văn Nam: Chuyên gia về hiện tượng tự nhiên, mang đến những bài viết dễ tiếp cận và hấp dẫn.
- Thảo Trang: Chuyên gia hình ảnh, đảm bảo nội dung trực quan và sinh động.
Cam kết minh bạch và Thông tin pháp lý
Chúng tôi cam kết mang đến một nền tảng minh bạch, nơi mọi thông tin đều được công khai và nội dung được kiểm chứng chặt chẽ. Vật Lý không chỉ là cổng thông tin tri thức mà còn là nơi bạn có thể tin tưởng tuyệt đối về tính chính xác và uy tín. Dưới đây là thông tin pháp lý chính thức của chúng tôi:
- Tên đơn vị: CÔNG TY TNHH GIÁO DỤC NT
- Mã số thuế: 3703292390
- Địa chỉ trụ sở: 22 Đ. D6, Tân Thuận Tây, Quận 765/1 khu phố Tân Hiệp, Phường Tân Đông Hiệp, TP Hồ Chí Minh, Việt Nam
- Hotline hỗ trợ: 0834950056
- Email liên hệ: [email protected]
Hãy cùng Vật Lý chinh phục mọi giới hạn của tri thức khoa học
Chúng tôi tin rằng, mỗi bước tiến trong hành trình học tập của bạn đều góp phần tạo nên tương lai tươi sáng hơn. Vật Lý luôn sẵn sàng đồng hành, cung cấp nguồn tài liệu phong phú và đáng tin cậy để bạn tự tin khám phá thế giới khoa học. Đừng ngần ngại tìm hiểu thêm về chúng tôi qua các trang Về chúng tôi, Chính sách bảo mật hoặc Điều khoản sử dụng để hiểu rõ hơn về cam kết của Vật Lý.
Hãy bắt đầu hành trình tri thức ngay hôm nay, cùng chúng tôi thắp sáng đam mê và chinh phục mọi thử thách. Vật Lý - nơi tri thức không có giới hạn!



![[Vật lý 7] Nhận biết ánh sáng - Nguồn sáng và vật sáng trong](https://vatly.edu.vn/uploads/400x300/2024/07/vat-ly-7-nhan-biet-anh-sang-nguon-sang-va-vat-sang-trong-400x300.webp)